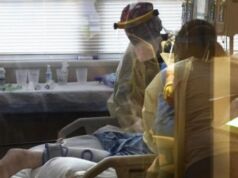
AstraZeneca a manqué la date limite de septembre pour son vaccin COVID-19 au Royaume-Uni, et il va fournir beaucoup moins de doses que promis d'ici la fin de l'année. Mais le PDG Pascal Soriot dit que les retards dans son essai clinique ont incité l'entreprise à retarder la fabrication.
"Les prédictions qui ont été faites de bonne foi à l'époque supposaient qu'absolument tout fonctionnerait et qu'il n'y avait aucun hoquet du tout", a déclaré Bingham aux législateurs, cité par le service de presse, faisant référence à un accord d'approvisionnement signé par AZ avec le Royaume-Uni. gouvernement en mai.

Réduction du temps, pas des coins: des processus intelligents à inclure dans le programme de développement clinique de phase 1 pour gagner du temps et des coûts tout en ajoutant de la valeur à votre actif clinique
Au cours de ce webinaire, les présentateurs passeront en revue les composants spécifiques de l'étude qui peuvent être très bénéfiques en termes de gain de temps et de coûts lorsqu'ils sont inclus dans une étude clinique de phase 1 / First-in-Man. Inscrivez-vous dès maintenant pour un aperçu perspicace pour toute personne novice dans les opérations de l'étude clinique de phase 1 et des informations utiles pour ceux qui n'ont pas exécuté de programme clinique précoce depuis un certain temps.
Le hoquet n'a pas été causé par l'incapacité d'AstraZeneca à produire suffisamment de vaccins, mais principalement en raison d'un ralentissement de l'essai clinique de phase 3 en cours, a déclaré Soriot jeudi lors d'un appel avec des journalistes.
Pour que l'essai clinique d'efficacité de phase 3 puisse être lu, il faudrait qu'un nombre suffisant de participants contractent le nouveau coronavirus au cours de leur vie quotidienne pour permettre aux chercheurs d'évaluer la capacité du candidat AZ à se protéger contre l'infection par rapport à une injection factice.
Lorsque AstraZeneca a signé le contrat britannique, les taux d'infection étaient à la hausse dans le grand public. Mais le nombre d’incidents a chuté au cours de l’été, ralentissant la progression du procès, a expliqué Soriot. Maintenant que les cas sont à nouveau en hausse, la société s'attend à avoir des données disponibles d'ici la fin de l'année, a-t-il déclaré.
CONNEXES : Le chef de l'essai conseille le vaccin AstraZeneca COVID-19 pour la baisse des données en 2020
Outre les incidents d’infection plus lents, la phase 3 du vaccin AZ a été temporairement interrompue pendant plus d’un mois après qu’un participant à l’essai ait développé une maladie neurologique grave. Le procès a obtenu le feu vert pour reprendre aux États-Unis fin octobre.
En raison des retards des essais, le calendrier prévu par AZ pour l’autorisation d’un vaccin a également été prolongé. Pour garantir que le produit final bénéficie d'une durée de conservation maximale au fur et à mesure que les doses sont déployées dans les campagnes de vaccination de masse, AZ a décidé de reporter sa livraison aux gouvernements, a déclaré Soriot.
En fait, AZ a déjà produit un vaccin en vrac qui est conservé à des températures de congélation. L'horloge de la durée de conservation commence à tourner une fois que la substance médicamenteuse congelée entre dans la phase de formulation de la production, a déclaré Pam Cheng, responsable des opérations et de l'informatique de la société.
La société est prête à fournir des produits commerciaux finis, a déclaré Cheng. «Cependant, nous devons vraiment être réfléchis à la façon dont nous progressons vers l'étape du produit final», a-t-elle déclaré. «Nous voulons avoir une durée de conservation maximale après approbation réglementaire dans le monde entier.»
À ce stade, il est préférable de conserver le vaccin dans cet état congelé, car il peut être conservé plus longtemps. Après avoir obtenu des données positives d'essais cliniques, AZ peut commencer à "remplir massivement des flacons, et nous serons prêts à fournir des centaines de millions de doses à partir de janvier de l'année prochaine", a déclaré Soriot aux journalistes.
Lorsque ce jour arrive, AZ peut fournir les doses sur une base continue selon un calendrier de livraison qui correspond au plan du gouvernement pour le rythme de la vaccination, a-t-il ajouté.
CONNEXES : AstraZeneca impose une limite de temps à son engagement " sans but lucratif " COVID-19 : rapport
La pharma britannique a construit une chaîne d'approvisionnement mondiale capable de produire 3 milliards de doses de vaccin. Il y a quelques semaines, l'entreprise a franchi le cap de la validation de ses processus, ce qui signifie qu'elle a établi une assurance qualité, la dernière étape avant la fabrication commerciale, a déclaré Soriot.
AZ s'est engagé à ne pas profiter du vaccin COVID-19 pendant la pandémie. En plus d'inclure les coûts de fabrication dans ce calcul, la société enregistre des coûts de plus d'un milliard de dollars provenant d'essais cliniques et d'autres activités. Pour s'assurer qu'il compense ces dépenses, AZ ajoute un montant équivalent à un maximum de 20% du coût de fabrication au prix du vaccin, a déclaré Soriot.
En plus des 100 millions de doses promises au gouvernement britannique, AZ a un contrat pour fournir 300 millions de doses aux États-Unis et un autre avec l'UE pour 400 millions de doses. Au Japon, la société a accepté de livrer 120 millions de doses. En Chine, le vaccin sera proposé par la société locale BioKangtai, qui réservera suffisamment de capacité pour fabriquer au moins 100 millions de doses d'ici la fin de 2020.