Par Julie Steenhuysen et Michael Erman
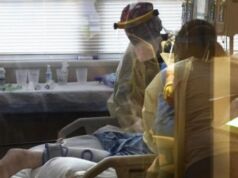
Les gens reçoivent des vaccins contre la maladie à coronavirus (COVID-19) à la station de métro du quartier Queens de New York
Les conseillers extérieurs de la Food and Drug Administration des États-Unis ont voté vendredi à l'unanimité pour recommander aux régulateurs d'autoriser une deuxième injection du vaccin COVID-19 de Johnson & Johnson pour mieux protéger les Américains qui ont reçu le vaccin à dose unique.
Erreur de chargement
Le comité consultatif sur les vaccins et les produits biologiques connexes de la FDA a soutenu les injections de tous les receveurs de J&J âgés de 18 ans et plus au moins deux mois après leur première dose.
La FDA n'est pas tenue de suivre les recommandations du comité consultatif, mais elle le fait généralement.
Après avoir entendu les présentations des scientifiques de J&J et de la FDA, de nombreux membres du comité consultatif ont demandé si le vaccin à dose unique de J&J devrait en fait être considéré comme un vaccin à deux doses pour tout le monde.
Ils ont souligné les niveaux inférieurs d'anticorps neutralisant le virus qu'il provoque par rapport aux vaccins utilisant la technologie d'ARN messager (ARNm) de Moderna Inc et Pfizer Inc/BioNTech SE
"Il y a un impératif de santé publique. Ce que nous constatons, c'est qu'il s'agit d'un groupe dont l'efficacité globale est inférieure à celle que nous avons vue avec le vaccin à ARNm, et il est donc urgent de faire quelque chose", a déclaré le Dr Arnold Monto, épidémiologiste. à l'École de santé publique de l'Université du Michigan qui a présidé la réunion.
Le Dr Peter Marks, directeur du Center for Biologics Evaluation and Research de la FDA, s'est dit préoccupé par le fait que les données présentées par J&J ne reflétaient pas toutes les informations sur les performances du vaccin.
Vidéo : les conseillers de la FDA se préparent à voter sur les boosters Moderna et J&J Covid (CNBC)
Les conseillers de la FDA se préparent à voter sur les boosters Moderna et J&J Covid
Cliquez pour agrandir
SUIVANT
"Il y a de vrais défis ici. Toutes les données ne correspondent pas pleinement au fait qu'il s'agit d'un vaccin qui conserve une excellente activité au fil du temps, contre toutes les formes de maladie ou même contre les formes graves de maladie", a déclaré Marks.
Les scientifiques de J&J ont déclaré que leur vaccin était plus durable que les vaccins à ARNm.
Le Dr Dan Barouch, un chercheur sur les vaccins de Harvard qui a aidé à concevoir le vaccin COVID-19 de J&J, a présenté les données d'une étude publiée vendredi dans le New England Journal of Medicine. Il a révélé que les niveaux d'anticorps du vaccin J&J étaient "sensiblement inférieurs" à ceux des deux vaccins à ARNm, mais que les réponses immunitaires restaient durables, "avec peu de preuves de déclin pendant plus de huit mois".
Le Dr Eric Rubin, expert en maladies infectieuses à la Harvard Chan School of Public Health, a déclaré : "Si le vaccin n'est pas adéquat, il devrait être renforcé et tout le monde devrait le recevoir."
Après le vote, Rubin a déclaré qu'il s'attend à ce que l'obtention de la deuxième dose plus de deux mois après la première soit sans danger. Bien que les données soient rares, a-t-il déclaré, "il n'y a pas grand-chose à suspecter que ce soit faux", ajoutant: "Je suis certainement favorable à ce que ces personnes reçoivent une autre dose".
Marks a déclaré que l'agence considérerait la demande du panel d'appeler le deuxième vaccin comme une dose supplémentaire plutôt qu'un rappel, reflétant l'opinion de nombreux membres du panel selon laquelle il aurait dû être un vaccin à deux injections depuis le début.
Une fois que la FDA aura approuvé la deuxième dose, les Centers for Disease Control and Prevention des États-Unis feront des recommandations spécifiques sur les personnes qui devraient recevoir les injections. Les conseillers du CDC doivent se réunir pour discuter des boosters la semaine prochaine.
Jeudi, le panel a soutenu à l'unanimité les injections de rappel https://www.reuters.com/business/healthcare-pharmaceuticals/us-fda-advisers-weigh-case-covid-19-vaccine-booster-shots-2021-10-14 du vaccin COVID-19 de Moderna pour les Américains âgés de 65 ans et plus et ceux à haut risque de maladie grave ou d'exposition professionnelle au virus.
Les agences de santé américaines ont autorisé le mois dernier les rappels du vaccin Pfizer/BioNTech.
Les autorités sanitaires américaines ont subi des pressions pour autoriser les injections supplémentaires après que la Maison Blanche a annoncé en août des plans pour une vaste campagne de rappel en attendant les approbations de la FDA et du CDC.
(Reportage de Manojna Maddipatla à Bangalore ; Montage par Caroline Humer et Bill Berkrot)